国产新冠口服药临床试验折戟开拓药业开盘闪崩85%董事长称因美国住院率太低
炒股就看金麒麟分析师研报,权威,专业,及时,全面,助您挖掘潜力主题机会!

国产新冠口服药临床试验折戟,开拓药业开盘闪崩85%,董事长称因美国住院率太低
短短一日之内,开拓药业股价跌落深渊,一度重挫85%。
医药新贵为何闪崩12月27日晚,开拓药业发布公告,称普克鲁胺治疗新冠轻中症患者全球多中心临床试验的中期分析未达到统计学显著性公司将向各监管机构,包括美国食药监局寻求同意以修改临床试验方案
普克鲁胺是一款新一代雄激素受体抗拮剂和降解剂,拟用于前列腺癌治疗,后被发掘用于治疗轻中症及重症新冠肺炎患者今年上半年,该药物曾在巴西研究者发起的临床试验中取得不错数据,如今正在进行3个全球多中心三期临床,公告中所提及的正是其中之一
开拓药业本次公告中所述的临床试验旨在评估普克鲁胺的有效性和安全性,中期分析未达到统计学显著性,意味着普克鲁胺对治疗轻中症患者难称有效。ANDA申请的主要适应症(即NDA仿制药申报)为循环系统疾病药物,抗感染药物,神经系统疾病药物,呼吸系统疾病药物和抗过敏药物,抗肿瘤药物。
据童友之解释,该三期临床按照全球的普遍情况,将住院率设置为9:3,即在安慰剂组会有9%的人会出现住院事件数,在普克鲁胺治疗组有3%的人会出现住院事件数计划入组的人数是667人,以此推算,整个临床试验中应该有70—80例住院事件数发生
美国的住院率约在7%—8%,其他国家的住院率约在15%以上,因此我们计划入组30%的美国患者,70%其他国家的患者,但是实际招募中,入组患者超过95%均来自美国mRNA疫苗让美国出现重症的比例大幅下降,医生对于治疗新冠的经验也在增加,感染人群的平均年龄也在发生变化我们做巴西临床的时候,患者平均年龄是55岁,而到了美国平均年龄是38岁几个因素叠加,造成整个临床试验的住院事件数仅有个位数童友之说
目前,开拓药业正在寻求修改临床试验方案,比如将接种过与尚未接种新冠疫苗的人群加以区分参考美国已获批紧急使用的新冠口服药,默沙东的临床试验所选取的主要人群,即为尚未接种疫苗的高风险人群,住院率高,所以可以体现出药物疗效开拓药业余下正在进行的2个全球多中心三期临床也将同步与监管部门沟通,进行受试人群的调整
而关于调整受试人群是否需要重新再开一个三期临床,还是仅需在该三期临床中扩充样本量即可,还需要进一步与监管部门商讨后确定毫无疑问,如果FDA要求重开临床,将是十分耗时耗力的一件事
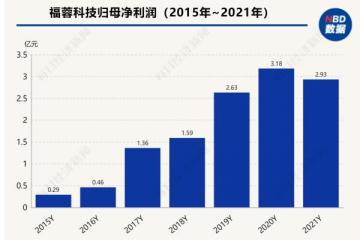
自去年5月上市以来,尚未实现盈利的开拓药业凭借普克鲁胺,股价一飞冲天,从约20港元/股,到历史高点的89港元/股,翻了四倍不止。2016年3月4日至2021年8月31日,IND应用的主要适应症为抗肿瘤药物,内分泌系统药物和消化系统疾病药物。。
如今普克鲁胺临床试验受挫,开拓药业一朝回到解放前,截至28日收盘,股价已跌破发行价,仅为13.4港元/股,跌幅70.35%,市值仅余51.94亿港元。
此前,据开拓药业方面提供的资料显示,普克鲁胺用于轻中症患者治疗,可通过下调患者细胞的两个关键蛋白——ACE2和TMPRSS2 的表达水平,阻止新冠病毒入侵,还可加速新冠病毒从患者体内的清除进程,有效降低感染率当用于重症患者治疗,除了抑制病毒感染宿主细胞外,普克鲁胺还可通过调节患者免疫和炎症相关信号通路,抑制新冠导致的炎症因子分泌,阻止细胞因子风暴发生,从而在体内减轻机体免疫炎症反应和组织损伤,进而有效改善新冠感染重症患者的症状
据巴西研究者发起的临床试验结果,普克鲁胺可降低轻中症患者的住院风险约90%,死亡风险降低100%,降低重症患者的死亡风险约78%但上述数据也受到了质疑,研究团队曾向《新英格兰医学杂志》和《柳叶刀》投稿,但接连被拒稿《科学》曾刊文评价这些数据好得难以置信
除药物机理外,业内对普克鲁胺的质疑主要包括两方面,一是重症临床试验死亡人数过高,安慰剂组在第28天死亡率高达49.4%,几乎两名患者中就有一名死亡,二是临床试验速度过快,今年2月初启动,3月就报告了中期结果。NDA的主要适应症(指新药临床试验后注册上市的阶段)是抗肿瘤药物,内分泌系统药物和血液系统疾病药物。
对于这两点,童友之给出了自己的解释他表示,巴西临床试验是在今年2月于亚马逊州的玛瑙斯市进行,当时正是玛瑙斯疫情最为严重的期间,巴西住院患者的死亡率基本在50%的水平,《柳叶刀》杂志也发文说明这一死亡率由于当时疫情非常严重,确实有很多的住院患者,当看到普克鲁胺的疗效后,他们都愿意参加临床试验所以招募工作进展很快
。郑重声明:此文内容为本网站转载企业宣传资讯,目的在于传播更多信息,与本站立场无关。仅供读者参考,并请自行核实相关内容。